朱康顺教授团队发现“消除肿瘤基质屏障,增强肝癌免疫治疗效果的新方法”

近日,广州医科大学附属第二医院微创介入科朱康顺教授团队,在肝癌免疫治疗方面取得新成果,通过“设计纳米药物降解肿瘤基质屏障、促进肿瘤内T细胞浸润和细胞毒性T淋巴细胞(CTL)增殖的方法,增强了PD-1单抗治疗肝癌的疗效”,该成果以原创性论著形式发表在国际著名SCI期刊《Journal of Controlled Release》(中科院医学一区,IF: 11.467)。
论文题目:Nanodrug removes physical barrier to promote T-cell infiltration for enhanced cancer immunotherapy. Journal of Controlled Release, 2023,356: 360-372. (纳米药物消除肿瘤基质屏障促进T细胞浸润增强肝癌免疫治疗效果)

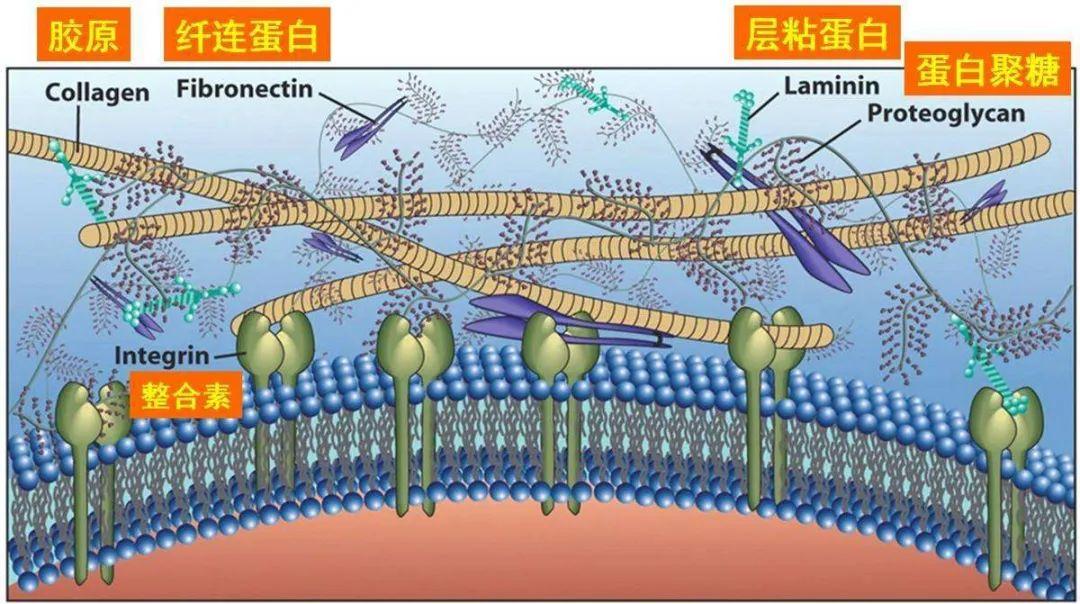
肝细胞癌(HCC)是最常见的恶性肿瘤之一,是癌症相关的第四大死亡原因。虽然目前免疫检查点抑制剂治疗在肿瘤免疫治疗中取得巨大进展,但其在肝细胞癌上的治疗效果仍有待提高。在HCC中,致密的细胞外基质(ECM)是CTL浸润肿瘤的关键障碍,严重影响了T细胞依赖性的免疫检查点抑制剂在HCC上的治疗效果。
基于此,朱康顺教授团队开发了一种基于磷酸钙(CaP)的纳米载体,用于输送透明质酸酶(HAase)、IL-12和抗PD-L1抗体(αPD-L1)。通过肿瘤微环境的酸性触发的CaP的解体释放用于降解细胞外基质HAase和促进T细胞增殖的IL-12,增强了肿瘤内T细胞的浸润和CTL的增殖。
此外,肿瘤微环境过度表达的MMP-2剪切用于连接αPD-L1的敏感多肽,在肿瘤微环境释放αPD-L1阻断免疫检查点,防止了肿瘤细胞逃避CTLs的杀伤作用。这种组合策略诱发了强大的抗肿瘤免疫力,有效地抑制了小鼠的HCC生长。而且,具有肿瘤微环境响应功能的聚乙二醇(PEG)涂层增强了纳米载体的肿瘤积累,并减少了由αPD-L1脱靶诱发的免疫相关不良事件(irAEs)。这种双敏感的纳米药物展示了一种有效的免疫治疗范式,并可能适用于其他具有ECM过度沉积特征的实体肿瘤(图1)。

图1-用于肝细胞癌免疫治疗的pH和MMP-2双重敏感的纳米药物的制备及肿瘤治疗机制示意图
来源:广医二院微创介入科
[注:本文部分图片来自互联网!未经授权,不得转载!每天跟着我们读更多的书]
互推传媒文章转载自第三方或本站原创生产,如需转载,请联系版权方授权,如有内容如侵犯了你的权益,请联系我们进行删除!
如若转载,请注明出处:http://www.hfwlcm.com/info/144175.html